发布时间:2026-01-06 10:43:20 编辑:小妹来源:网络
IB化学都学什么?IB化学课程难在哪里?其实IB化学学不动,根源就是知识断层+方法错位!这里我们针对IB化学进行详细分享,此外犀牛教育针对IB化学也开设多种课程,详情咨询文末小助手!
IB化学的学习内容虽然分为SL和HL:
HL与SL的核心区别
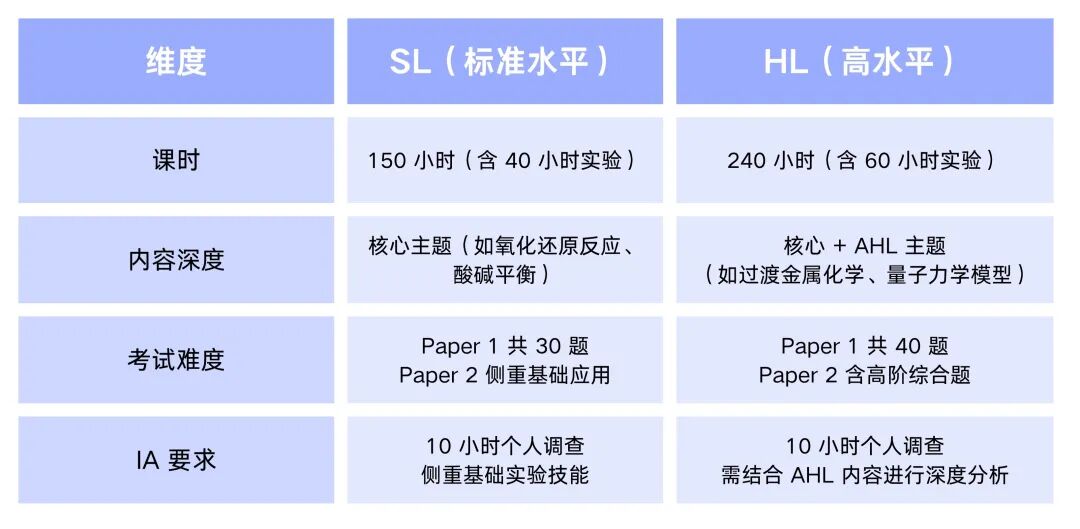
但是都是要学习以下四个板块,分别是:化学原理、物理化学、有机化学和无机化学。
化学原理是化学学科的核心理论基础,换句话说就是让我们认识到化学是什么的一个学科。学生会学习到物质的组成、结构、性质、变化规律以及化学反应的本质和机制,比如原子结构原理,物质的熔沸点、周期表中半径、电离能、电负性的规律等等。
物理化学是一门交叉学科,主要是研究化学物质的物理性质、物理变化以及化学过程中物理因素的科学,内容涉及物质的化学反应,化学键的性质和行为,热力学和电动力学等。考察题型除了简答题,也会涉及到计算题,譬如能量的计算,平衡的计算,等等。
有机化学又称为碳化合物的化学,研究的主要是含碳化合物的组成、结构、性质、制备方法及应用的科学,和我们的生活息息相关。
有机之外的,就是无机化学,主要研究无机化合物的组成、结构、性质、反应及其应用,比如金属,空气当中的氧、氮气等。
作为一门基础性自然科学课程,IB化学的难度主要体现在其对综合能力的高要求,具体可归纳为以下几点:
IB化学涉及的知识面相当广泛,涵盖氧化还原、有机化学、能量学、化学动力学、热化学、原子结构、化学键与物质结构等核心模块,许多主题是相互联系的,如果学生早期化学概念理解不到位,在后续的IB化学学习中可能会带来极大困难。
IB化学与物理、数学、生物等科目相互交叉和关联,考试中涉及定量计算(如化学计量学相关题型),热力学中的能量守恒定律、热量传递,生物体内有机化合物(蛋白质、核酸、糖类等)的结构和功能,这种跨学科的融合也增加了学习的复杂性。
IB化学概念偏抽象,要求学生富有想象力的思维才能理解(如分子构型、反应机理),此外有机化学等模块涉及物质性质及反应规律等,需要学生做好大量记忆的准备,并要能把这些知识点灵活应用于陌生情境。
高频考点:滴定计算(包括反滴定)、气体定律应用(如STP下体积换算)、氧化还原反应配平。
易错点:单位换算(如dm³与m³、g与kg)、有效数字保留、过量反应物判断。
技巧:通过“摩尔桥”模型(物质的量→质量/体积/浓度)串联计算步骤,结合真题总结典型题型(如含杂质的纯度计算)。
例题训练:

核心概念:电子排布(如Cr、Cu的异常电子构型)、电离能与电负性的周期性变化。
HL扩展:轨道能级分裂(如d轨道的晶体场理论)、光谱与能级跃迁(如氢原子发射光谱的计算)。
真题趋势:结合元素周期表位置分析性质差异(如第三周期元素的熔沸点变化)。
例题训练:

关键模型:VSEPR理论预测分子几何构型、杂化轨道(如sp³、sp²、sp)。
HL难点:分子轨道理论(如σ键与π键的形成)、金属键的自由电子模型。
实验关联:通过熔沸点差异判断作用力类型(如氢键对水的影响)。
例题训练:
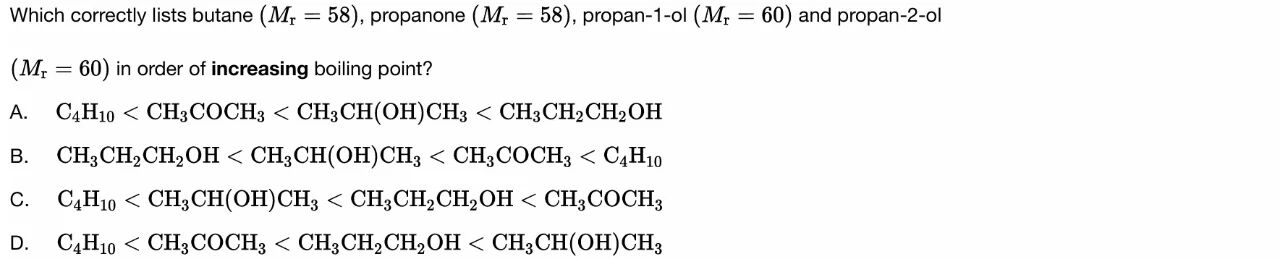
计算核心:焓变(ΔH)的测定(如中和热、燃烧热)、Hess定律的应用。
HL进阶:熵变(ΔS)与吉布斯自由能(ΔG)的计算,判断反应自发性。
常见错误:符号错误(放热ΔH为负)、状态符号(s/l/g)的遗漏。
例题训练:

反应速率:碰撞理论、活化能(Eₐ)的实验测定(如lnkvs1/T的斜率)。
平衡原理:LeChatelier原理的定性分析(如浓度、温度、压强对平衡的影响)。
HL计算:平衡常数(Kc/Kp)的表达式与数值计算,涉及ICE表格的应用。
例题训练:

围绕考试大纲建立知识框架,采用模块化方法整合内容,按原子结构→化学键→热力学→有机化学模块梳理知识点,通过构建跨章节知识网络图强化概念间的逻辑关联。
针对考试重点内容进行专项突破,比如有机反应机理(亲电取代、亲核加成)、热力学计算(焓变、熵变),每个知识单元学习后,通过完成对应教材习题来检验掌握程度。

AMC01-19


物理碗01-19

物理碗01-18

